(2023·郑州高一检测)下列有机物和乙醇具有相同官能团的是( )
- A: 苯乙烯(
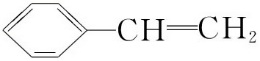 )
) - B: 丙三醇(
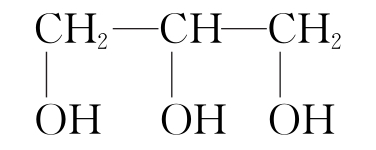 )
) - C: 丙酮(
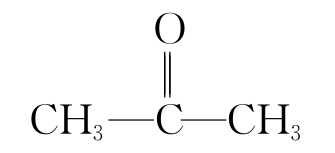 )
) - D: 乙醚(CH3CH2—O—CH2CH3)
苯乙烯含有![]() ,官能团和乙醇不同;丙三醇含有—OH,官能团和乙醇相同;丙酮含有
,官能团和乙醇不同;丙三醇含有—OH,官能团和乙醇相同;丙酮含有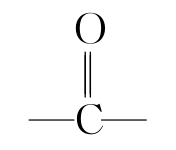 ,官能团和乙醇不同;乙醚含有
,官能团和乙醇不同;乙醚含有![]() ,官能团和乙醇不同。
,官能团和乙醇不同。
我国明代《本草纲目》中收载药物1 892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”此法利用下列乙醇的哪项性质( )
由信息可知,“蒸令气上……其清如水,味极浓烈”,所得到的是乙醇,利用的是乙醇易挥发的性质。
(2024·长春高一月考)下列关于乙醇的说法错误的是( )
下列有机物不属于烃的衍生物的是( )
根据烃和烃的衍生物的定义进行分析判断,烃中只含有碳、氢元素,而烃的衍生物中还含有其他元素。
(2023·郑州高一检测)下列有机物和乙醇具有相同官能团的是( )
 )
) )
)苯乙烯含有![]() ,官能团和乙醇不同;丙三醇含有—OH,官能团和乙醇相同;丙酮含有
,官能团和乙醇不同;丙三醇含有—OH,官能团和乙醇相同;丙酮含有 ,官能团和乙醇不同;乙醚含有
,官能团和乙醇不同;乙醚含有![]() ,官能团和乙醇不同。
,官能团和乙醇不同。
(2024·杭州高一段考)女儿红是传统名酒,属于发酵酒中的黄酒,用糯米、红糖等发酵而成,除乙醇外,还含有大量人体所需的氨基酸,江南的冬天空气潮湿寒冷,人们常饮用此酒来增强抵抗力。下列有关酒精的说法中正确的是( )
乙醇发生催化氧化反应生成醛,乙醇中碳氢键、氢氧键断裂,A错误;乙醇结构中有—OH,但不能电离,故不是碱,B错误;Na置换出羟基中的氢原子,烃基上的氢原子不能被置换出来,C错误。
C2H5OH的官能团是—OH,含有—OH的物质具有与乙醇相似的化学性质,在Cu或Ag的催化下,下列物质不能与O2发生催化氧化反应的是( )
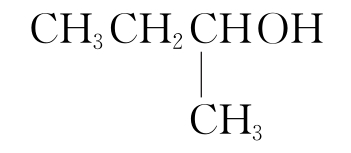
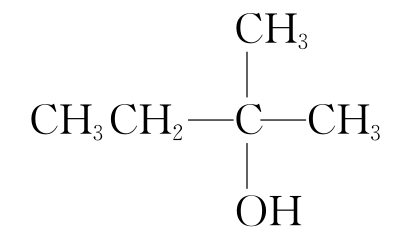
A、B、C项分子中与羟基相连的碳原子上均有氢原子,均能发生催化氧化反应;D项, 分子中与羟基相连的碳原子上没有氢原子,不能发生催化氧化反应。
分子中与羟基相连的碳原子上没有氢原子,不能发生催化氧化反应。
已知分子中含有羟基的物质都能与钠反应生成氢气。乙醇、乙二醇(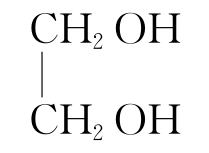 )、丙三醇(
)、丙三醇(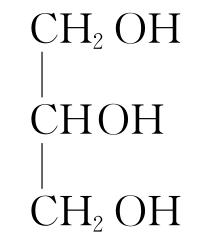 )分别与足量钠反应,产生等量的氢气。则三种醇的物质的量之比为( )
)分别与足量钠反应,产生等量的氢气。则三种醇的物质的量之比为( )
羟基个数与被置换的氢原子个数之比为1∶1,三种醇与钠反应放出等量的氢气,则三种醇提供的羟基数目相同,因此三种醇的物质的量之比为1∶∶=6∶3∶2。
乙醇是生活中常见的有机物。下列有关如图所示乙醇的实验的说法错误的是( )
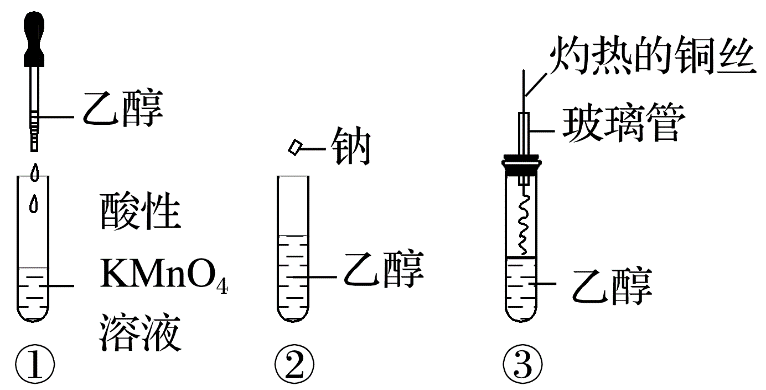
向酸性KMnO4溶液中滴加乙醇,乙醇被氧化为乙酸,酸性KMnO4溶液褪色,A项错误;乙醇的密度比钠的小,故钠先沉在乙醇底部,乙醇中含有羟基,能与金属钠反应生成氢气,试管中有气泡产生,B项正确;灼热的铜丝与O2反应生成黑色的CuO,将其插入乙醇中又会被乙醇还原为金属铜,由黑色变为红色,C项正确;图③是乙醇的催化氧化反应,铜作催化剂,D项正确。
某有机物的结构简式为CH3CH==CHCH2OH,下列有关该物质说法正确的是( )
分子式为C4H8O,A错误;该分子中含烷基,所有原子不可能共平面,B错误;该分子中含碳碳双键,能发生加成反应,烷基上含氢原子,能发生取代反应,C正确;—CH2OH也能使酸性高锰酸钾溶液褪色,不能用酸性KMnO4溶液检验该物质中的碳碳双键,D错误。
香叶醇是合成玫瑰香油的主要原料,其键线式如图所示。下列有关香叶醇的叙述正确的是( )
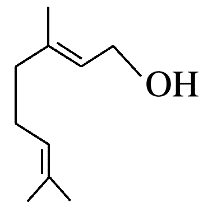
A项,由香叶醇的结构简式可得分子式为C10H18O;分子中含有碳碳双键,能使溴的CCl4溶液褪色,能使酸性高锰酸钾溶液紫红色褪去,B、C错误;D项,分子中碳碳双键可发生加成反应,烃基中的氢原子可发生取代反应。
已知分子结构中含有—OH的有机物可以和钠反应放出氢气,某实验小组为了测定乙醇的结构式是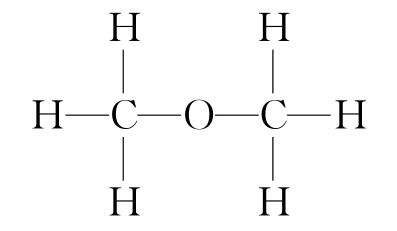 还是
还是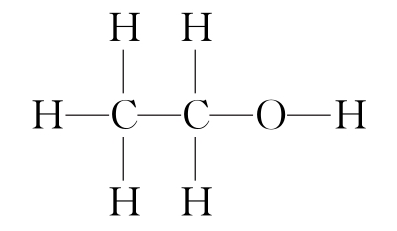 ,利用乙醇和钠的反应,设计如图装置进行实验探究:
,利用乙醇和钠的反应,设计如图装置进行实验探究:
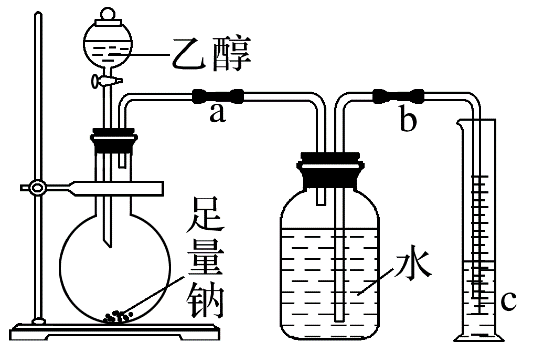
(1)实验前检查该装置的气密性的实验操作是________________________________。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为________(填“正确”或“不正确”)。
(3)如果实验开始前b导管内未充满水,实验结束后b导管内充满水,则实验结果将________(填“偏大”或“偏小”)。
(4)若测得有1.15 g C2H6O参加反应,把量筒c中水的体积换算成标准状况下H2的体积为280 mL,试结合计算进行讨论,判断下面Ⅰ和Ⅱ中,哪个是乙醇的结构式?________(填“Ⅰ”或“Ⅱ”)。
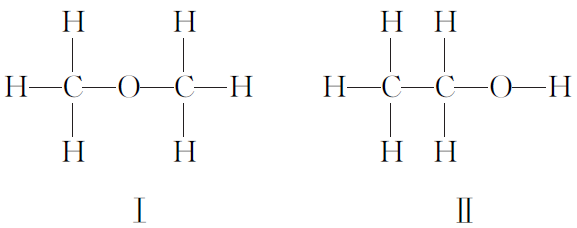
答案: (1)连接好装置,关闭分液漏斗的活塞,将右侧导管插入水槽,微热烧瓶,右侧导管若有气泡冒出,冷却后形成一段水柱,且一段时间内水柱无变化,证明装置气密性良好 (2)不正确 (3)偏小 (4)Ⅱ
该实验的关键是准确测量反应产生气体的体积,根据产生气体的体积可以确定被置换的氢原子的个数。(2)虽然装置中存在空气,但只有生成氢气时,才会改变装置内气体的压强,从而使水进入量筒中,排出水的体积等于氢气的体积,与装置内空气的体积无关,故该说法不正确。(4)参加反应的乙醇的物质的量是=0.025 mol,生成氢气的物质的量是=0.012 5 mol,即乙醇分子中的6个氢原子的类型并不完全相同,有1个应不同于其他的氢原子,从而确定乙醇的结构式为Ⅱ。
生活中的有机物种类丰富,在衣食住行多方面应用广泛,其中乙醇是比较常见的有机物。
(1)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为 ,该反应类型是 。
(2)下列属于乙醇的同系物的是 (填字母,下同),属于乙醇的同分异构体的是 。
A.![]() B.
B.![]()
C.乙醚(CH3CH2OCH2CH3) D.甲醇(CH3OH)
E.CH3—O—CH3 F.HO—CH2CH2—OH
(3)46 g乙醇完全燃烧消耗 mol氧气。
(4)下列四种有机物的分子式都是C4H10O ,其中不能被氧化为同碳原子数的醛的是 (填字母)。
A.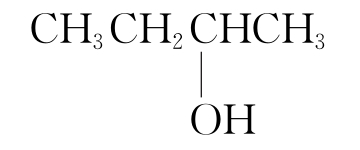 B.
B.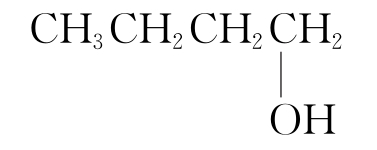
C.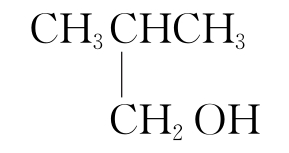 D.
D.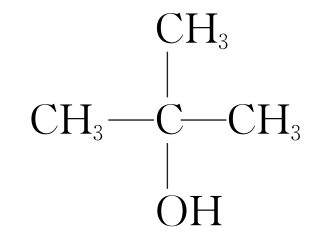
答案: (1)CH2==CH2+H2O![]() CH3CH2OH 加成反应 (2)D E (3)3 (4)AD
CH3CH2OH 加成反应 (2)D E (3)3 (4)AD
(1)乙烯和水在催化剂、加热、加压条件下生成乙醇的反应类型为加成反应,该反应的化学方程式为CH2==CH2+H2O![]() CH3CH2OH。(3)根据乙醇燃烧的化学方程式CH3CH2OH+3O2
CH3CH2OH。(3)根据乙醇燃烧的化学方程式CH3CH2OH+3O2![]() 2CO2+3H2O可知,46 g乙醇即1 mol乙醇,完全燃烧消耗3 mol O2。(4)醇分子结构中有“—CH2OH”的可被氧化为同碳原子数的醛,故选AD。
2CO2+3H2O可知,46 g乙醇即1 mol乙醇,完全燃烧消耗3 mol O2。(4)醇分子结构中有“—CH2OH”的可被氧化为同碳原子数的醛,故选AD。